
微信扫一扫
关注公众号
公司新闻
案例解析 | 抗病毒生物大分子制药治疗
发布时间:2020-03-12 15:34 | 点击次数:722
近期爆发的新型冠状病毒肺炎(COVID-19,对应的病毒为 SARS-CoV-2)突出了开发有效治疗方法的重要性。在近期的公众号中,我们向大家介绍了「人民的希望」瑞德西韦的工作机制 [1],在此,我们结合疫苗、血清、多肽和单抗的研究案例,向大家继续介绍靶向病毒的大分子治疗和我们的解决方案是如何推动下一代治疗研究的。
No.1 针对 MERS 的疫苗优化研究
中东呼吸综合征冠状病毒 (MERS-CoV),是近年来第二个造成大规模人群传染的冠状病毒,相较于 SARS 病毒,其致死率高、发病快,因此急需研发有效的疫苗用于被动免疫。在 2015 年由 NIH 的 Barney S. Graham 主导的研究中,科学家评价和比较了靶向 MERS 的多种疫苗方案 [2]。

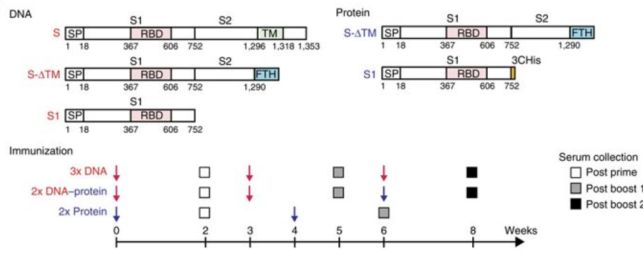
基于 DNA 和蛋白为免疫原的免疫流程,图片源自参考资料 2。
围绕 MERS 冠状病毒的刺突蛋白 (S),研究构建了多种 cDNA 和蛋白免疫原,分别通过电转和配合佐剂的形式免疫小鼠。为了提升研究的安全性,科学家建立了带有化学发光报告基因的假病毒体系。通过检测由病毒感染所致的化学发光,研究利用可溶性 DPP4(MERS 靶点)和 DPP4 抗体验证了假病毒的功能。
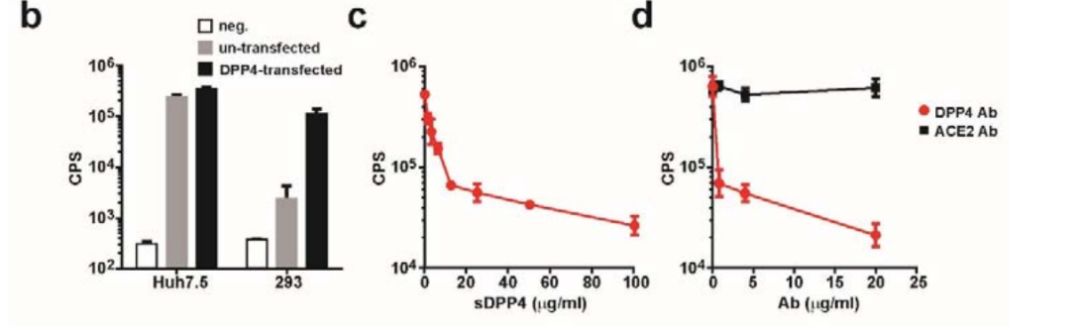
MERS 假病毒功能性验证,左图:基于过表达技术验证 DPP4 过表达提升病毒的感染能力,Huh7.5 内源性高表达 DPP4。中图:基于可溶性 DPP4 的竞争实验。右图:利用 DPP4 抗体抑制假病毒的感染。假病毒的化学发光检测基于 96-well white/black Isoplate 微孔板和 Microbeta 平台。图片源自参考资料 2。
借助假病毒体系,研究追踪和评价了不同免疫策略产生的血清的中和能力和针对多种 MERS 病毒株的交叉中和能力。从结果可以看出,全程 S1 蛋白和 2X S DNA-S1 蛋白的免疫方案所获得的抗体最为有效,且能中和多种 MERS 病毒株。通过进一步的竞争实验和血清吸附实验,研究证实不同的免疫流程得到的血清靶向的 S 蛋白位置也不一样。与经典的微量中和实验 (Microneutralization) 相比,研究证实假病毒体系评价抗体中和能力更为敏感,灵敏度约有一个数量级的提升。通过解析抗体的亚型,研究发现基于 S DNA 的免疫方案能诱导 IgG2a 为主导的免疫反应,而 S1 蛋白刺激则产生 IgG1 为主导的免疫反应。在小鼠中,IgG2a 的出现反映了 Th1 型免疫反应,促进了抗病毒相关因子如 interferon-γ的释放,提升了 T 细胞介导的抗病毒反应。因此,相较于蛋白,基于 DNA 的疫苗可以通过建立 T 辅助细胞免疫应答来更有效的控制病毒感染。
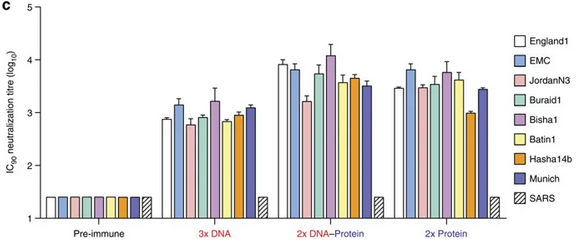
血清的交叉中和能力检测。假病毒的化学发光检测基于 96-well white/black Isoplate 微孔板和 Microbeta 平台。图片源自参考资料 2。
对应的,在非人灵长类动物(印度恒河猴)模型上,全程 S1 蛋白和 2X S DNA-S1 蛋白的免疫方案产生的中和抗体滴度优越于基于全程 DNA 的免疫方案。病毒接种后,相较于对照组,免疫组动物显著降低肺部病理指标。疫苗中 DNA 免疫原的引入更是进一步缓解肺部的损伤情况,并加速了康复过程。
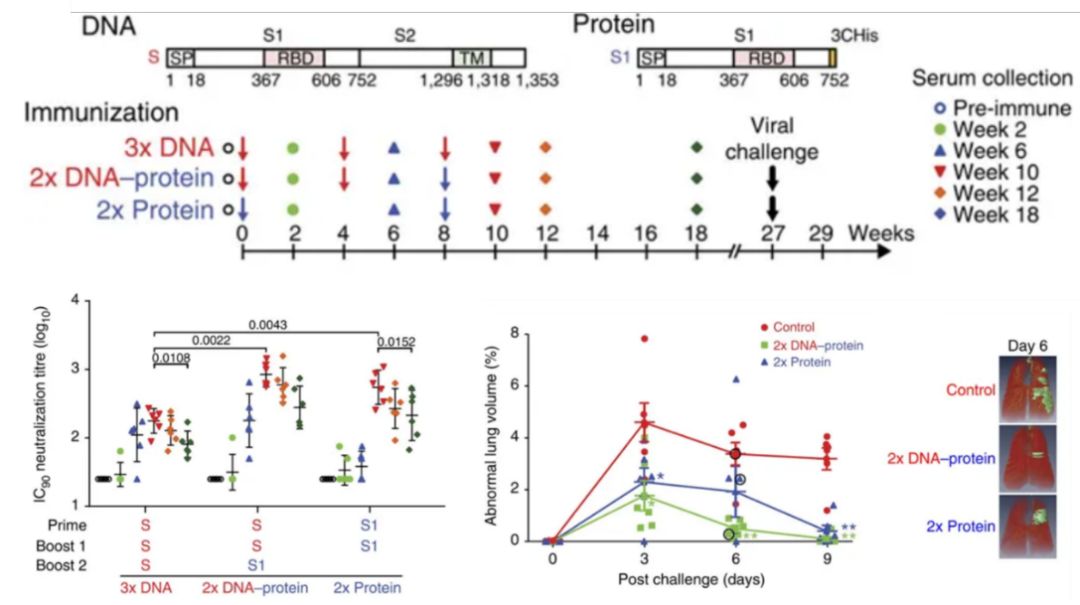
基于非人灵长类动物(印度恒河猴)模型的疫苗评价。上图:免疫流程。下左图:动物血清中和实验,基于 96-well white/black Isoplate 微孔板和 Microbeta 平台。下右图:通过 CT 评价疫苗的保护作用。图片源自参考资料 2。
No.2 基于转基因牛的抗病毒血清研究
在抗击 SARS 和流感的临床疗法中,「恢复期血浆」治疗 (Convalescent‑phase plasma therapy) 获得了一定的成效,有效降低了死亡率。但是,该法的疗效很大程度上依赖于是否能及时获得有效的血清。相比下,基于动物的超免疫血清虽然能解决量的问题,但其使用可能会导致严重的免疫反应和毒性。单克隆抗体疗法,又一种基于被动免疫的治疗方法,面临耗时长和出现耐药突变病毒株等挑战。
为了解决上述的问题,有研究人员将目光转向了转基因牛 (Transchromosomic (Tc) bovines) 来快速获得大量、有效的抗病毒血清。通过基因工程,研究人员敲除牛自身的 IgG,并引入完整的、可指定 IgG 亚型人抗体表达体系,来达到免疫系统人源化的效果。免疫后的牛每只每月可提供高达 150 到 600 g 的人 IgG。目前,已有多项临床前研究利用该技术对抗 MERS 和 Ebola 等传染病 [3,4]。在此,我们着重介绍靶向 MERS 的研究。

在免疫原段,该研究利用了两种材料:灭活的 Jordan 病毒株 (WKVV) 和基于 Al-Hasa 病毒株 S 蛋白的纳米材料 (SPNV)。两种免疫原均能刺激产生 S 蛋白特异的血清和人 IgG(SAB-300/301)。基于安全性和生产可行性等因素,研究主要围绕基于 SPNV 产生的人 IgG 开展动物和临床研究。
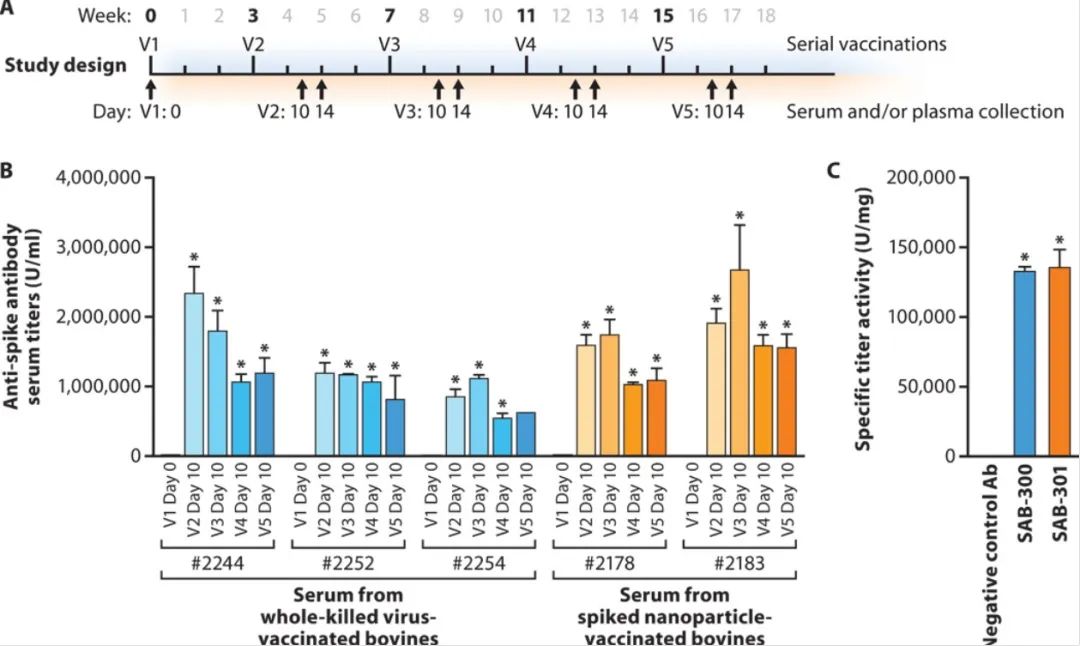
上图:基于转基因牛的免疫过程。下图:利用 Anti-Spike 抗体检测所得血清(左)和纯化人 IgG(右)的有效含量。图片源自参考资料 3。
除了特异性检测外,研究利用免疫荧光成像技术,结合 Anti-Spike 抗体来衡量免疫所得血清和抗体的抗病毒中和作用 (FRNA50)。相较于只能完成一轮感染的假病毒体系,FRNA50 能直观、全面地反映药物处理对于病毒感染能力的影响。在该研究中,此法还结合 mRNA 检测验证病毒的灭活效果,确保疫苗的安全性。结合 FRNA50 和传统的半数组织培养感染量 (Tissue culture infectious dose-50%,TCID50) 测定法,研究证明纯化的血清含有高水平的中和多抗。在过表达 DPP4 的小鼠模型上,无论是预防性还是治疗性给药,SAB-301 都能有效的控制肺部的病毒量。在安全性上,SAB-301 不支持抗体依赖的病毒感染增强作用 (Antibody-dependent enhancement,ADE)。目前,由 SAB Biotherapeutics 公司推出的 SAB-301 已进入一期临床试验。
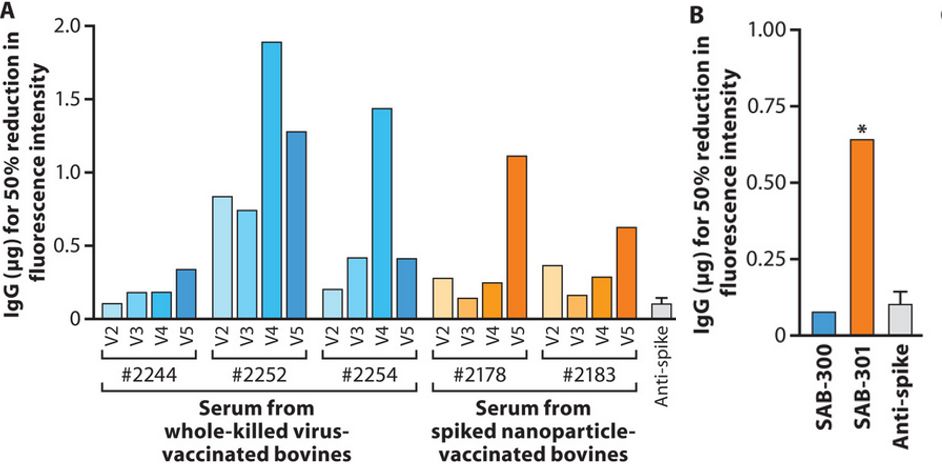
利用 FRNA50 检测所得血清(左)和纯化人 IgG(右)靶向 MERS 病毒的中和能力。FRNA50 基于 Operetta 高内涵平台和配套微孔板。图片源自参考资料 3。
No.3 利用 ADCC 抗击 H7N9 禽流感的单抗研究
作为肿瘤免疫疗法的主要推动者,单克隆抗体(单抗)也被广泛用于抗击 SARS 和 HIV 等多种病毒的研究中。此外,基于 HIV-1 和流感中和单抗的研究也为疫苗设计提供了新的思路。但是,基于杂交瘤技术的传统单抗制备面临着耗时长,步骤多且繁琐等问题,限制了其对可能出现的新型疫情爆发的应对能力。相比下,噬菌体展示技术为快读获得高亲和力人源单抗提供了新的途径。基于该技术平台,复旦大学研究人员建立超大型天然全人源抗体库,并成功鉴定靶向 MERS 和流感的强力抗体 [5,6]。

在抗击 H7N9 流感的工作中,为了获得低突变的高特异抗体,研究人员以重组表达的 HA 和 HA1 蛋白为抗原,基于健康人 B 细胞来源的天然抗体库开展多轮筛选,获得单抗 m826。经序列分析,研究人员证明 m826 与胚系基因高度同源,是胚系抗体。相较于体细胞高度突变的抗体,胚系抗体建立时间短,安全性高且成药性更好,适用于靶向急性感染的抗体和疫苗研发。
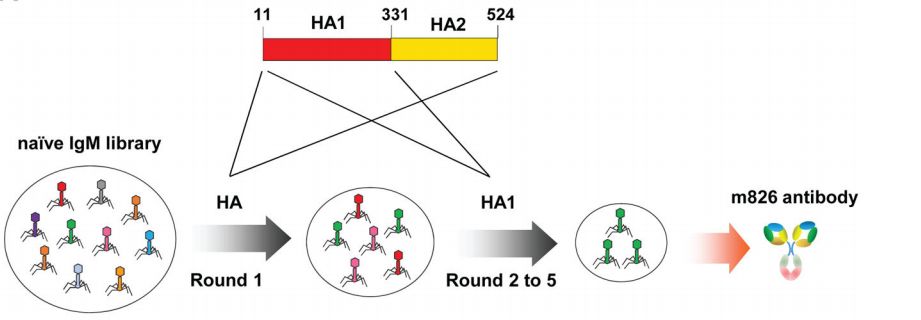
基于噬菌体展示技术的 H7N9 抗体筛选,图片源自参考资料 6。
非常有意思的是,在红细胞凝集抑制 (Hemagglutination inhibition,HI) 反应中,m826 仅表现出微弱的抗病毒能力。进一步的细胞病变效应 (Cytopathic effect,CPE) 检测和免疫荧光法中和实验证明 m826 不能中和流感病毒,抑制其在靶细胞的增殖。利用亲脂性荧光染料 R18 和 SP-DiOC18(3)来标记病毒,研究发现 m826 对病毒与靶细胞的结合和膜融合过程无显著影响。但是,m826 能很强结合表达 H7N9 HA 蛋白的细胞,是 ADCC(Antibody-dependent cell-mediated cytotoxicity,抗体依赖的细胞介导的细胞毒性作用)活力的强力介导者。同时,由于不能中和 H7N9 病毒,m826 还能成为高价值的工具性抗体。在动物模型上,IgG1 m826 能有效的预防和控制 H7N9 的感染。因此,m826 依赖于 ADCC,而不是中和能力抗击流感病毒。这一发现为抗病毒抗体的筛选和研发提供了新的思路和途径。
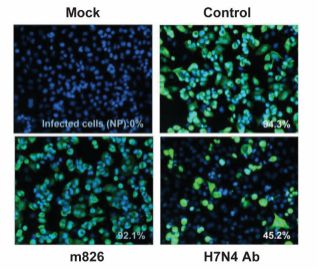
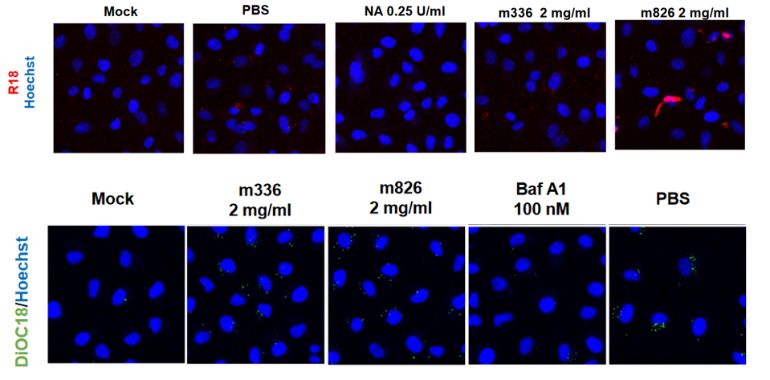
左图:基于免疫荧光成像技术(荧光标记病毒)的中和实验,H7N4 抗体为中和阳性对照。右上:病毒结合检测,红色荧光探针 R18 标记病毒,感染 30 分钟后进行成像检测。NA 为结合阴性对照;m336 为阴性对照抗体。右下:利用荧光探针 R18 和 SP-DiOC18(3)双标记病毒,病毒膜融合发生会诱导 SP-DiOC18(3)绿色荧光信号加强。Baf A1 为融合阴性对照。上述高通量成像检测均基于 Opera 或 Operetta 高内涵平台。图片源自参考资料 6。
No.4 靶向膜融合的广谱抗病毒多肽研究
作为动物来源的病毒,冠状病毒因其多样性,较高的传播能力和进化能力限制了单一的靶向疗法的临床应用。因此,从长远角度来看,能作用于多种冠状病毒的新型广谱抗病毒药物,会成为抗击流行性和新型冠状病毒感染的终极武器。相较于高度变异的受体结合区 (Receptor-binding domain, RBD),病毒膜融合涉及的 Heptad repeat (HR) 区高度保守。同时膜融合也是病毒感染和复制重要的功能性过程。因此,该区域成为了抑制性多肽的研究重点。靶向冠状病毒的膜融合过程,来自于复旦大学的研究团队研发出广谱多肽抑制剂 EK1,为抗击冠状病毒和类似病毒提供了新的大分子治疗策略 [7]。

冠状病毒可通过胞内体膜融合途径 (Endosomal pathway) 或/和细胞表面胞浆膜融合途径 (Non-endosomal pathway) 进入细胞。病毒通过结合宿主细胞受体激活其 S2 亚基的 HR1 和 HR2 区,互相结合形成对膜融合至关重要的 6-HB(Six-helix bundle) 结构。
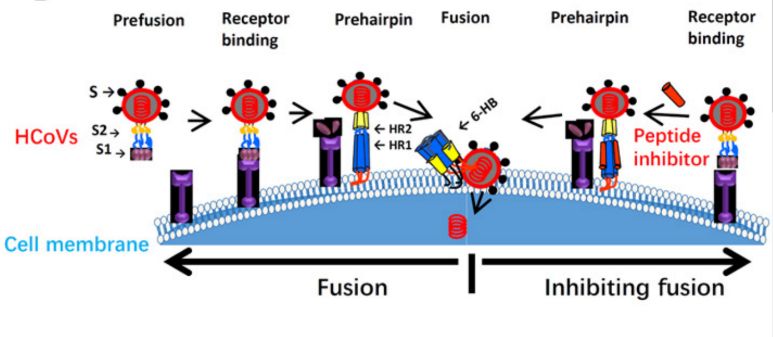
冠状病毒的膜融合过程和竞争性多肽工作机制,图片源自参考资料 7。
鉴于此,研究人员以多种冠状病毒的保守 HR 区为模板,合成 HR1 和 HR2 区来源的多肽(HR1P 和 HR2P)用于竞争。通过过表达技术,研究进一步建立靶向多种冠状病毒的细胞细胞融合实验,系统性筛查 HR1P 和 HR2P 对细胞融合的抑制。结果显示由 OC43 株来源的 HR2P 具有广谱且强效的抑制融合能力。在此基础上,研究人员通过引入氨基酸和突变等方法,进一步优化多肽的可溶性和成药性。所获得的多肽 EK1,在进一步的一系列体外检测,包括细胞细胞融合实验,假病毒法,Blam-Vpr 法和活病毒增殖能力检测中,都表现出强效的广谱抗病毒能力。
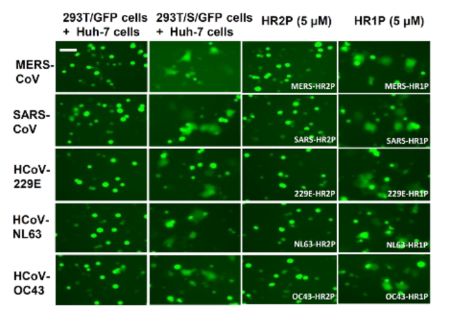
细胞细胞融合实验,过表达病毒 S 蛋白并带有 GFP 信号的 293T 细胞为作用细胞,Huh-7 为靶细胞,图片源自参考资料 7。
除了可以用于免疫缺陷和老年患者外,多肽类药物的另一优势是支持非侵入性鼻腔给药,适合用于靶向呼吸道的病毒感染。因此,检测鼻腔给药下的 EK1 的体内分布非常重要。基于活体成像技术,研究观察到 Cy5 荧光标记的 EK1 可广泛分布于整个呼吸道中,并集中在肺部。此外,一些肺外的器官,包括肝脏、肾和脾,都能检测到 EK1 的分布,表明 EK1 可以进入血液循环系统和其他脏器中。因此,EK1 还可能作用于由冠状病毒导致的系统性或多器官感染。在 OC43 和 MERS 感染小鼠模型上,EK1 均表现出强力的抗病毒能力,有效抑制了因感染带来的体重减轻和死亡现象。从体外到体内的多方面安全性评价表明通过鼻腔给药的 EK1 是低免疫原性,安全的治疗策略。因此,EK1 是一个新型、有潜力的广谱抗冠状病毒药物,值得进一步的深入研究。
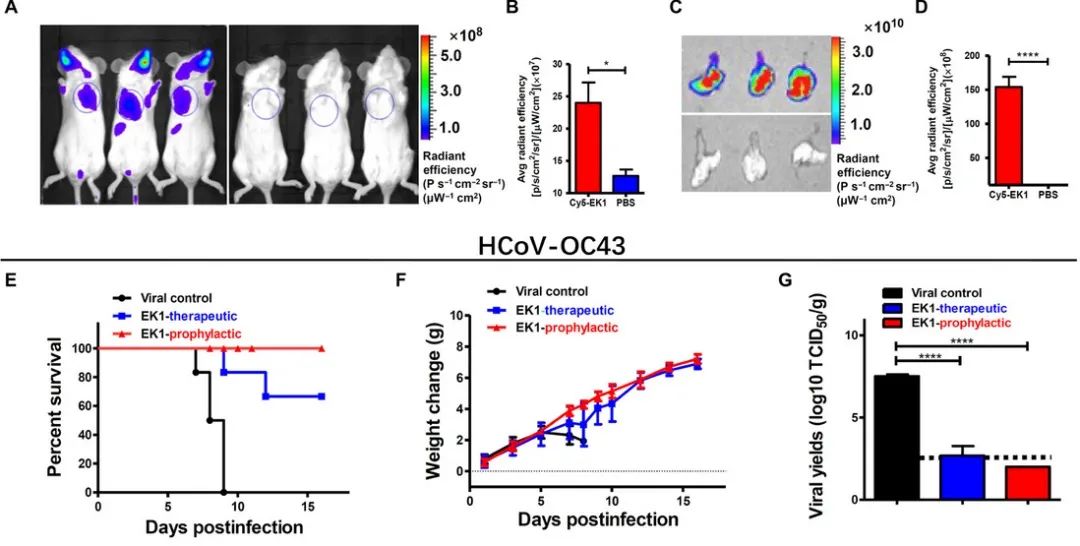
上:基于活体成像检测鼻腔给药下 Cy5 标记的 EK1 在小鼠体内的分布;小动物活体成像检测基于 IVIS 平台。下:EK1 处理对模型鼠死亡率、体重和病毒滴度的影响,图片源自参考资料 7。
总结
通过上述四个案例,我们总体介绍了靶向病毒段的大分子疗法的研究流程和关注点。助力此类治疗方法的研发,珀金埃尔默提供成熟的整体应用解决方案。针对携带萤火虫报告基因的假病毒研究,我们提供全面、配套的涵盖化学发光试剂,微孔板和高通量检测平台的解决方案。对于基于慢病毒包装系统的假病毒,我们还可以提供 p24 检测解决方案,用于快速衡量病毒的感染能力。此外,基于成像平台的解决方案,我们还可以分析短程和长程的复杂亚细胞活动,例如由病毒介导的膜融合过程。在血清和抗体的筛查和分析中,强大的高内涵解决方案能最大程度发挥表型筛选的优势,发现具有中和能力、安全的潜在抗体。同时,ADCC,作为关键的抗感染抗体工作机制之一,也是我们的主要应用关注点。针对 ADCC 的检测,我们提供金标准、灵活的放射和非放射解决方案,助力抗体类药物的深入评价 [8]。最后,在临床前动物研究中,除了中和检测外,我们提供覆盖功能到结构的活体成像解决方案,助力病理检测、药物分析和药效评价等核心工作。
参考文献
1. 药物机制解读 | 「人民的希望」抗病毒药物瑞德西韦 (Remdesivir)https://mp.weixin.qq.com/s/MyJO1XjkD6uQAgsoMFTxEw
2. Wang L, et al. Evaluation of candidate vaccine approaches for MERS-CoV. Nat Commun. 2015 Jul 28;6:7712.
3. Luke T, et al. Human polyclonal immunoglobulin G from transchromosomic bovines inhibits MERS-CoV in vivo. Sci Transl Med. 2016 Feb 17;8(326):326ra21.
4. Thomas Luke, et al. Fully Human Immunoglobulin G From Transchromosomic Bovines Treats Nonhuman Primates Infected With Ebola Virus Makona Isolate. J Infect Dis. 2018 Dec 15; 218(Suppl 5): S636–S648.
5. Ying T, et al. Junctional and allele-specific residues are critical for MERS-CoV neutralization by an exceptionally potent germline-like antibody. Nat Commun. 2015 Sep 15;6:8223.
6. Fei Yu,et al. A potent germline-like human monoclonal antibody targets a pH-sensitive epitope on H7N9 influenza hemagglutinin. Cell Host Microbe. 2017 Oct 11; 22(4): 471–483.e5.
7. Shuai Xia,et al. A pan-coronavirus fusion inhibitor targeting the HR1 domain of human coronavirus spike. Sci Adv. 2019 Apr; 5(4): eaav4580
8. DELFIA 经典技术应用于单抗研发及细胞治疗——AD0116 细胞杀伤专题之 ADCChttps://mp.weixin.qq.com/s/0lkBdDHL5MFIyoeoFV4wWQ
No.1 针对 MERS 的疫苗优化研究
中东呼吸综合征冠状病毒 (MERS-CoV),是近年来第二个造成大规模人群传染的冠状病毒,相较于 SARS 病毒,其致死率高、发病快,因此急需研发有效的疫苗用于被动免疫。在 2015 年由 NIH 的 Barney S. Graham 主导的研究中,科学家评价和比较了靶向 MERS 的多种疫苗方案 [2]。


基于 DNA 和蛋白为免疫原的免疫流程,图片源自参考资料 2。
围绕 MERS 冠状病毒的刺突蛋白 (S),研究构建了多种 cDNA 和蛋白免疫原,分别通过电转和配合佐剂的形式免疫小鼠。为了提升研究的安全性,科学家建立了带有化学发光报告基因的假病毒体系。通过检测由病毒感染所致的化学发光,研究利用可溶性 DPP4(MERS 靶点)和 DPP4 抗体验证了假病毒的功能。

MERS 假病毒功能性验证,左图:基于过表达技术验证 DPP4 过表达提升病毒的感染能力,Huh7.5 内源性高表达 DPP4。中图:基于可溶性 DPP4 的竞争实验。右图:利用 DPP4 抗体抑制假病毒的感染。假病毒的化学发光检测基于 96-well white/black Isoplate 微孔板和 Microbeta 平台。图片源自参考资料 2。
借助假病毒体系,研究追踪和评价了不同免疫策略产生的血清的中和能力和针对多种 MERS 病毒株的交叉中和能力。从结果可以看出,全程 S1 蛋白和 2X S DNA-S1 蛋白的免疫方案所获得的抗体最为有效,且能中和多种 MERS 病毒株。通过进一步的竞争实验和血清吸附实验,研究证实不同的免疫流程得到的血清靶向的 S 蛋白位置也不一样。与经典的微量中和实验 (Microneutralization) 相比,研究证实假病毒体系评价抗体中和能力更为敏感,灵敏度约有一个数量级的提升。通过解析抗体的亚型,研究发现基于 S DNA 的免疫方案能诱导 IgG2a 为主导的免疫反应,而 S1 蛋白刺激则产生 IgG1 为主导的免疫反应。在小鼠中,IgG2a 的出现反映了 Th1 型免疫反应,促进了抗病毒相关因子如 interferon-γ的释放,提升了 T 细胞介导的抗病毒反应。因此,相较于蛋白,基于 DNA 的疫苗可以通过建立 T 辅助细胞免疫应答来更有效的控制病毒感染。

血清的交叉中和能力检测。假病毒的化学发光检测基于 96-well white/black Isoplate 微孔板和 Microbeta 平台。图片源自参考资料 2。
对应的,在非人灵长类动物(印度恒河猴)模型上,全程 S1 蛋白和 2X S DNA-S1 蛋白的免疫方案产生的中和抗体滴度优越于基于全程 DNA 的免疫方案。病毒接种后,相较于对照组,免疫组动物显著降低肺部病理指标。疫苗中 DNA 免疫原的引入更是进一步缓解肺部的损伤情况,并加速了康复过程。

基于非人灵长类动物(印度恒河猴)模型的疫苗评价。上图:免疫流程。下左图:动物血清中和实验,基于 96-well white/black Isoplate 微孔板和 Microbeta 平台。下右图:通过 CT 评价疫苗的保护作用。图片源自参考资料 2。
No.2 基于转基因牛的抗病毒血清研究
在抗击 SARS 和流感的临床疗法中,「恢复期血浆」治疗 (Convalescent‑phase plasma therapy) 获得了一定的成效,有效降低了死亡率。但是,该法的疗效很大程度上依赖于是否能及时获得有效的血清。相比下,基于动物的超免疫血清虽然能解决量的问题,但其使用可能会导致严重的免疫反应和毒性。单克隆抗体疗法,又一种基于被动免疫的治疗方法,面临耗时长和出现耐药突变病毒株等挑战。
为了解决上述的问题,有研究人员将目光转向了转基因牛 (Transchromosomic (Tc) bovines) 来快速获得大量、有效的抗病毒血清。通过基因工程,研究人员敲除牛自身的 IgG,并引入完整的、可指定 IgG 亚型人抗体表达体系,来达到免疫系统人源化的效果。免疫后的牛每只每月可提供高达 150 到 600 g 的人 IgG。目前,已有多项临床前研究利用该技术对抗 MERS 和 Ebola 等传染病 [3,4]。在此,我们着重介绍靶向 MERS 的研究。

在免疫原段,该研究利用了两种材料:灭活的 Jordan 病毒株 (WKVV) 和基于 Al-Hasa 病毒株 S 蛋白的纳米材料 (SPNV)。两种免疫原均能刺激产生 S 蛋白特异的血清和人 IgG(SAB-300/301)。基于安全性和生产可行性等因素,研究主要围绕基于 SPNV 产生的人 IgG 开展动物和临床研究。

上图:基于转基因牛的免疫过程。下图:利用 Anti-Spike 抗体检测所得血清(左)和纯化人 IgG(右)的有效含量。图片源自参考资料 3。
除了特异性检测外,研究利用免疫荧光成像技术,结合 Anti-Spike 抗体来衡量免疫所得血清和抗体的抗病毒中和作用 (FRNA50)。相较于只能完成一轮感染的假病毒体系,FRNA50 能直观、全面地反映药物处理对于病毒感染能力的影响。在该研究中,此法还结合 mRNA 检测验证病毒的灭活效果,确保疫苗的安全性。结合 FRNA50 和传统的半数组织培养感染量 (Tissue culture infectious dose-50%,TCID50) 测定法,研究证明纯化的血清含有高水平的中和多抗。在过表达 DPP4 的小鼠模型上,无论是预防性还是治疗性给药,SAB-301 都能有效的控制肺部的病毒量。在安全性上,SAB-301 不支持抗体依赖的病毒感染增强作用 (Antibody-dependent enhancement,ADE)。目前,由 SAB Biotherapeutics 公司推出的 SAB-301 已进入一期临床试验。

利用 FRNA50 检测所得血清(左)和纯化人 IgG(右)靶向 MERS 病毒的中和能力。FRNA50 基于 Operetta 高内涵平台和配套微孔板。图片源自参考资料 3。
No.3 利用 ADCC 抗击 H7N9 禽流感的单抗研究
作为肿瘤免疫疗法的主要推动者,单克隆抗体(单抗)也被广泛用于抗击 SARS 和 HIV 等多种病毒的研究中。此外,基于 HIV-1 和流感中和单抗的研究也为疫苗设计提供了新的思路。但是,基于杂交瘤技术的传统单抗制备面临着耗时长,步骤多且繁琐等问题,限制了其对可能出现的新型疫情爆发的应对能力。相比下,噬菌体展示技术为快读获得高亲和力人源单抗提供了新的途径。基于该技术平台,复旦大学研究人员建立超大型天然全人源抗体库,并成功鉴定靶向 MERS 和流感的强力抗体 [5,6]。

在抗击 H7N9 流感的工作中,为了获得低突变的高特异抗体,研究人员以重组表达的 HA 和 HA1 蛋白为抗原,基于健康人 B 细胞来源的天然抗体库开展多轮筛选,获得单抗 m826。经序列分析,研究人员证明 m826 与胚系基因高度同源,是胚系抗体。相较于体细胞高度突变的抗体,胚系抗体建立时间短,安全性高且成药性更好,适用于靶向急性感染的抗体和疫苗研发。

基于噬菌体展示技术的 H7N9 抗体筛选,图片源自参考资料 6。
非常有意思的是,在红细胞凝集抑制 (Hemagglutination inhibition,HI) 反应中,m826 仅表现出微弱的抗病毒能力。进一步的细胞病变效应 (Cytopathic effect,CPE) 检测和免疫荧光法中和实验证明 m826 不能中和流感病毒,抑制其在靶细胞的增殖。利用亲脂性荧光染料 R18 和 SP-DiOC18(3)来标记病毒,研究发现 m826 对病毒与靶细胞的结合和膜融合过程无显著影响。但是,m826 能很强结合表达 H7N9 HA 蛋白的细胞,是 ADCC(Antibody-dependent cell-mediated cytotoxicity,抗体依赖的细胞介导的细胞毒性作用)活力的强力介导者。同时,由于不能中和 H7N9 病毒,m826 还能成为高价值的工具性抗体。在动物模型上,IgG1 m826 能有效的预防和控制 H7N9 的感染。因此,m826 依赖于 ADCC,而不是中和能力抗击流感病毒。这一发现为抗病毒抗体的筛选和研发提供了新的思路和途径。


左图:基于免疫荧光成像技术(荧光标记病毒)的中和实验,H7N4 抗体为中和阳性对照。右上:病毒结合检测,红色荧光探针 R18 标记病毒,感染 30 分钟后进行成像检测。NA 为结合阴性对照;m336 为阴性对照抗体。右下:利用荧光探针 R18 和 SP-DiOC18(3)双标记病毒,病毒膜融合发生会诱导 SP-DiOC18(3)绿色荧光信号加强。Baf A1 为融合阴性对照。上述高通量成像检测均基于 Opera 或 Operetta 高内涵平台。图片源自参考资料 6。
No.4 靶向膜融合的广谱抗病毒多肽研究
作为动物来源的病毒,冠状病毒因其多样性,较高的传播能力和进化能力限制了单一的靶向疗法的临床应用。因此,从长远角度来看,能作用于多种冠状病毒的新型广谱抗病毒药物,会成为抗击流行性和新型冠状病毒感染的终极武器。相较于高度变异的受体结合区 (Receptor-binding domain, RBD),病毒膜融合涉及的 Heptad repeat (HR) 区高度保守。同时膜融合也是病毒感染和复制重要的功能性过程。因此,该区域成为了抑制性多肽的研究重点。靶向冠状病毒的膜融合过程,来自于复旦大学的研究团队研发出广谱多肽抑制剂 EK1,为抗击冠状病毒和类似病毒提供了新的大分子治疗策略 [7]。

冠状病毒可通过胞内体膜融合途径 (Endosomal pathway) 或/和细胞表面胞浆膜融合途径 (Non-endosomal pathway) 进入细胞。病毒通过结合宿主细胞受体激活其 S2 亚基的 HR1 和 HR2 区,互相结合形成对膜融合至关重要的 6-HB(Six-helix bundle) 结构。

冠状病毒的膜融合过程和竞争性多肽工作机制,图片源自参考资料 7。
鉴于此,研究人员以多种冠状病毒的保守 HR 区为模板,合成 HR1 和 HR2 区来源的多肽(HR1P 和 HR2P)用于竞争。通过过表达技术,研究进一步建立靶向多种冠状病毒的细胞细胞融合实验,系统性筛查 HR1P 和 HR2P 对细胞融合的抑制。结果显示由 OC43 株来源的 HR2P 具有广谱且强效的抑制融合能力。在此基础上,研究人员通过引入氨基酸和突变等方法,进一步优化多肽的可溶性和成药性。所获得的多肽 EK1,在进一步的一系列体外检测,包括细胞细胞融合实验,假病毒法,Blam-Vpr 法和活病毒增殖能力检测中,都表现出强效的广谱抗病毒能力。

细胞细胞融合实验,过表达病毒 S 蛋白并带有 GFP 信号的 293T 细胞为作用细胞,Huh-7 为靶细胞,图片源自参考资料 7。
除了可以用于免疫缺陷和老年患者外,多肽类药物的另一优势是支持非侵入性鼻腔给药,适合用于靶向呼吸道的病毒感染。因此,检测鼻腔给药下的 EK1 的体内分布非常重要。基于活体成像技术,研究观察到 Cy5 荧光标记的 EK1 可广泛分布于整个呼吸道中,并集中在肺部。此外,一些肺外的器官,包括肝脏、肾和脾,都能检测到 EK1 的分布,表明 EK1 可以进入血液循环系统和其他脏器中。因此,EK1 还可能作用于由冠状病毒导致的系统性或多器官感染。在 OC43 和 MERS 感染小鼠模型上,EK1 均表现出强力的抗病毒能力,有效抑制了因感染带来的体重减轻和死亡现象。从体外到体内的多方面安全性评价表明通过鼻腔给药的 EK1 是低免疫原性,安全的治疗策略。因此,EK1 是一个新型、有潜力的广谱抗冠状病毒药物,值得进一步的深入研究。

上:基于活体成像检测鼻腔给药下 Cy5 标记的 EK1 在小鼠体内的分布;小动物活体成像检测基于 IVIS 平台。下:EK1 处理对模型鼠死亡率、体重和病毒滴度的影响,图片源自参考资料 7。
总结
通过上述四个案例,我们总体介绍了靶向病毒段的大分子疗法的研究流程和关注点。助力此类治疗方法的研发,珀金埃尔默提供成熟的整体应用解决方案。针对携带萤火虫报告基因的假病毒研究,我们提供全面、配套的涵盖化学发光试剂,微孔板和高通量检测平台的解决方案。对于基于慢病毒包装系统的假病毒,我们还可以提供 p24 检测解决方案,用于快速衡量病毒的感染能力。此外,基于成像平台的解决方案,我们还可以分析短程和长程的复杂亚细胞活动,例如由病毒介导的膜融合过程。在血清和抗体的筛查和分析中,强大的高内涵解决方案能最大程度发挥表型筛选的优势,发现具有中和能力、安全的潜在抗体。同时,ADCC,作为关键的抗感染抗体工作机制之一,也是我们的主要应用关注点。针对 ADCC 的检测,我们提供金标准、灵活的放射和非放射解决方案,助力抗体类药物的深入评价 [8]。最后,在临床前动物研究中,除了中和检测外,我们提供覆盖功能到结构的活体成像解决方案,助力病理检测、药物分析和药效评价等核心工作。
参考文献
1. 药物机制解读 | 「人民的希望」抗病毒药物瑞德西韦 (Remdesivir)https://mp.weixin.qq.com/s/MyJO1XjkD6uQAgsoMFTxEw
2. Wang L, et al. Evaluation of candidate vaccine approaches for MERS-CoV. Nat Commun. 2015 Jul 28;6:7712.
3. Luke T, et al. Human polyclonal immunoglobulin G from transchromosomic bovines inhibits MERS-CoV in vivo. Sci Transl Med. 2016 Feb 17;8(326):326ra21.
4. Thomas Luke, et al. Fully Human Immunoglobulin G From Transchromosomic Bovines Treats Nonhuman Primates Infected With Ebola Virus Makona Isolate. J Infect Dis. 2018 Dec 15; 218(Suppl 5): S636–S648.
5. Ying T, et al. Junctional and allele-specific residues are critical for MERS-CoV neutralization by an exceptionally potent germline-like antibody. Nat Commun. 2015 Sep 15;6:8223.
6. Fei Yu,et al. A potent germline-like human monoclonal antibody targets a pH-sensitive epitope on H7N9 influenza hemagglutinin. Cell Host Microbe. 2017 Oct 11; 22(4): 471–483.e5.
7. Shuai Xia,et al. A pan-coronavirus fusion inhibitor targeting the HR1 domain of human coronavirus spike. Sci Adv. 2019 Apr; 5(4): eaav4580
8. DELFIA 经典技术应用于单抗研发及细胞治疗——AD0116 细胞杀伤专题之 ADCChttps://mp.weixin.qq.com/s/0lkBdDHL5MFIyoeoFV4wWQ

